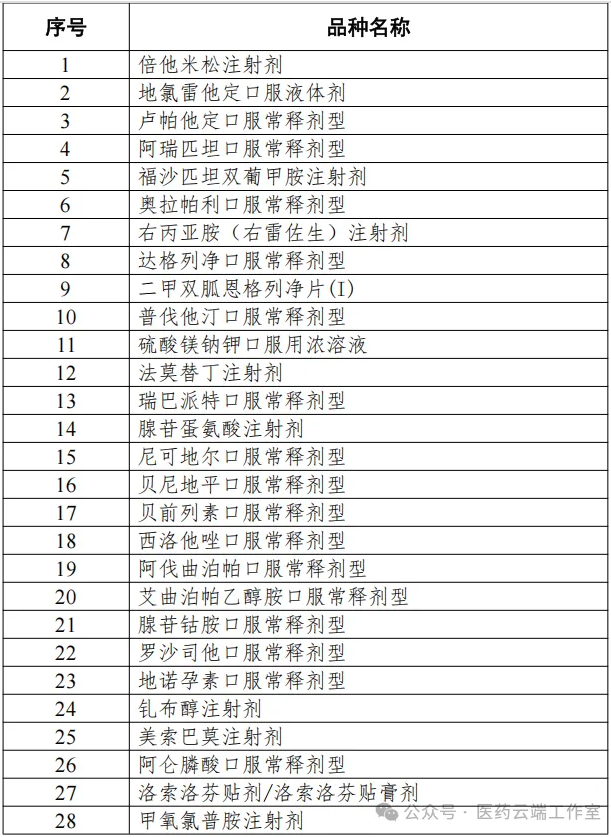
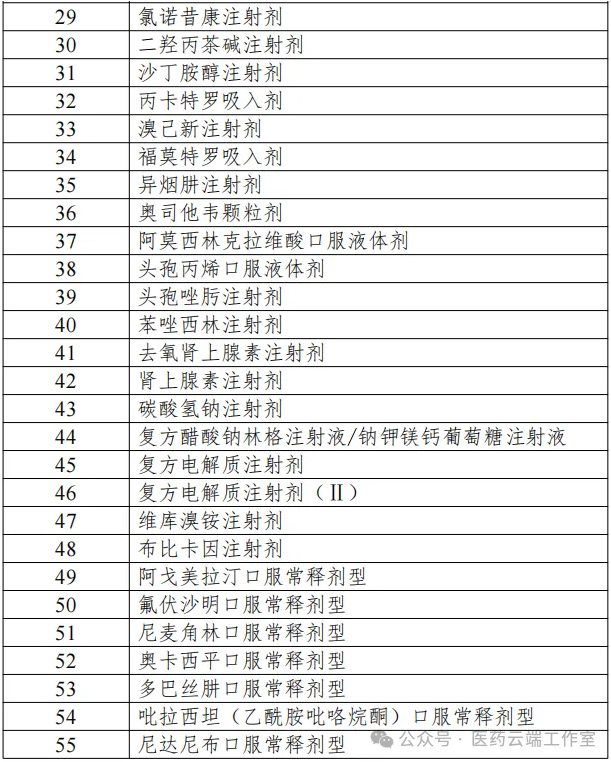
??? 7月15日,國家組織藥品聯合采購辦公室發布通知,啟動第11批國家組織藥品集中采購相關藥品信息填報工作,并公布擬納入第11批集采的清單,共計55個品種。
??? 當天,國家醫保局召開媒體通氣會,介紹優化集采的措施。據了解,本次集采優化了品種遴選條件。55個品種如何而來?
??? 會上,國家組織藥品聯合采購辦公室(以下簡稱國家組織藥品聯采辦)主任鄭頤作了詳細解讀。“按照要求,我辦以2025年3月31日為時間節點,沿用第10批集采‘參比制劑和通過一致性評價仿制藥企業數達到7家及以上’作為第11批集采的品種遴選條件。”
??? 鄭頤介紹,品種信息來源包括三個方面:
??? 一是中國醫藥工業信息中心提供的國家藥監局化學藥品目錄集(內含參比制劑和過評藥品信息),二是國家藥監局公開發布的仿制藥參比制劑目錄(內含參比制劑信息),三是米內數據庫的一致性評價進度信息(內含過評藥品信息)。三方面來源的數據互為補充,取并集匯總后滿足遴選條件品種數有122個。
??? 在此基礎上,國家組織藥品聯合采購辦公室對擬納入品種進行遴選,主要包括三個步驟。
??? 第一步:結合醫保目錄、市場規模等進行篩選。
??? 鄭頤介紹,第11批集采聚焦臨床使用成熟、市場競爭充分的品種,更好發揮集采的規模效應,在滿足遴選條件的基礎上,結合既往品種遴選規則和集采政策優化要求,排除存在以下情形的品種:
??? 一是主要成分、給藥途徑和適應證相同但包含醫保目錄內品規和目錄外品規的“跨醫保目錄”品種,區分為醫保內、外分組采購,區分后不滿足競爭格局的,不納入。
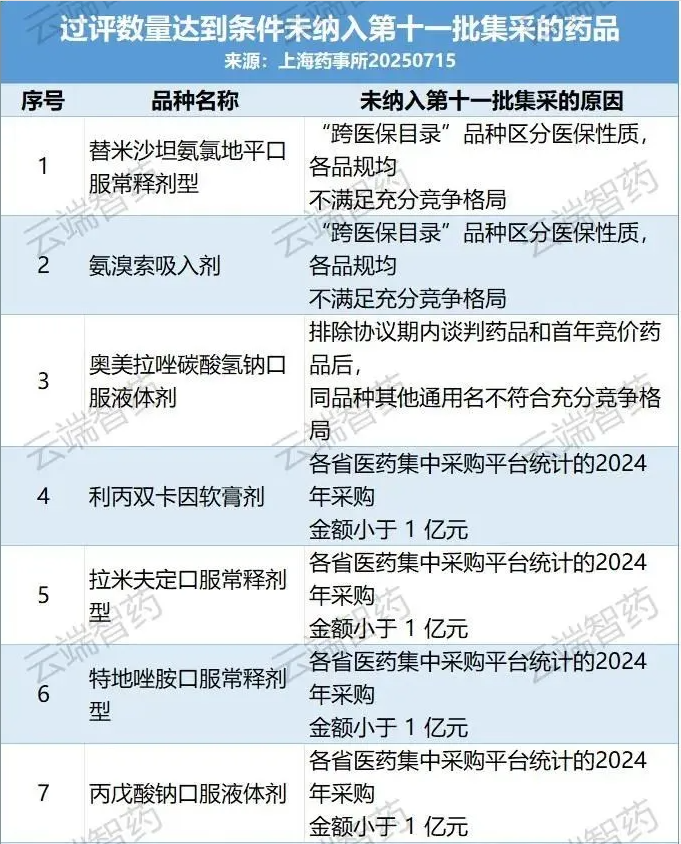
??? 此種情形共排除了替米沙坦氨氯地平口服常釋劑型、氨溴索吸入劑2個品種,以及復方電解質注射劑、二甲雙胍恩格列凈口服常釋劑型等7個品種的部分品規。
??? 如替米沙坦氨氯地平口服常釋劑型(總格局1+6,即參比制劑有1家企業,通過一致性評價有7家企業,下同),同屬口服常釋劑型的有2個品規,分別為替米沙坦氨氯地平片(1+4,醫保)和替米沙坦氨氯地平片(Ⅱ)(0+4,自費),區分醫保和自費性質后2個品規均未滿足競爭格局,按此情形替米沙坦氨氯地平口服常釋劑型不納入。“
??? 此條遴選規則也是為了保障患者醫保報銷的公平性,使用同一集采品種的不同患者的報銷屬性相同。”鄭頤說。
??? 二是協議期內的國家醫保談判藥品、新進入醫保目錄首年的競價藥品不納入,共排除奧美拉唑碳酸氫鈉口服液體劑1個品種以及復方氨基酸注射劑、二甲雙胍恩格列凈口服常釋劑型等3個品種的部分品規。
??? 參照最新版《國家基本醫療保險、工傷保險和生育保險藥品目錄(2024年)》,國家醫保目錄中談判藥品協議期內暫不納入集采,競價藥品沿用既往規則在新進入醫保目錄首年暫不納入集采,次年如符合條件則納入集采。
??? 如奧美拉唑碳酸氫鈉口服液體劑的“(Ⅱ)”品規在談判協議期內,去除該品規后,其余品規競爭格局為“0+6”,不符合競爭格局條件,故該品種不納入。二甲雙胍恩格列凈口服常釋劑型的“(Ⅲ)”“(Ⅵ)”品規處于首年競價藥品,不納入,去除該2品規后,其余品規仍滿足競爭格局條件,保留。
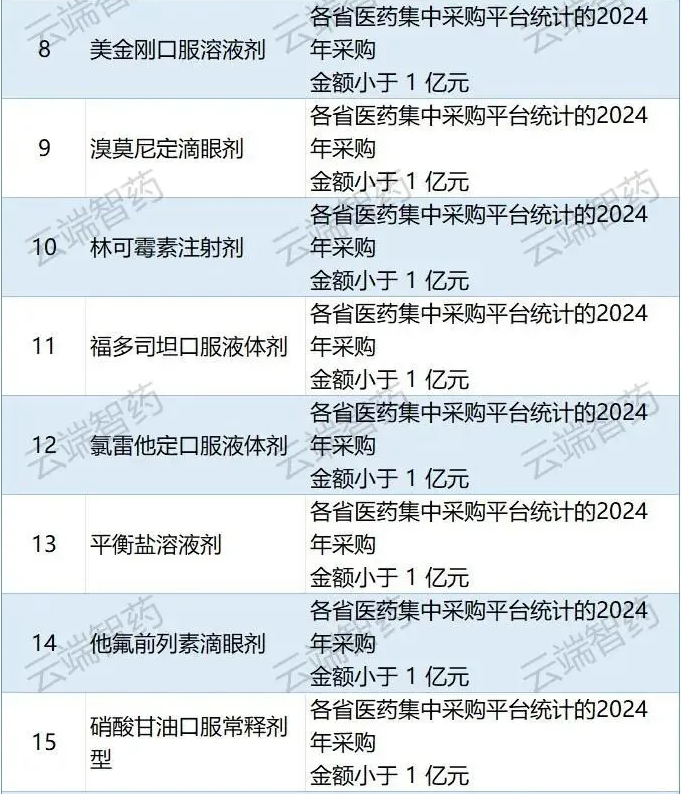
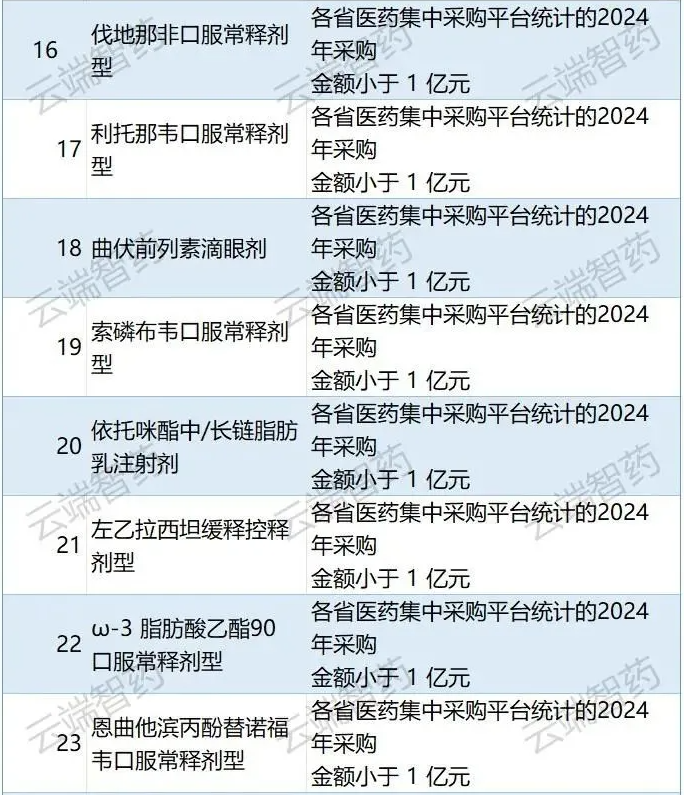
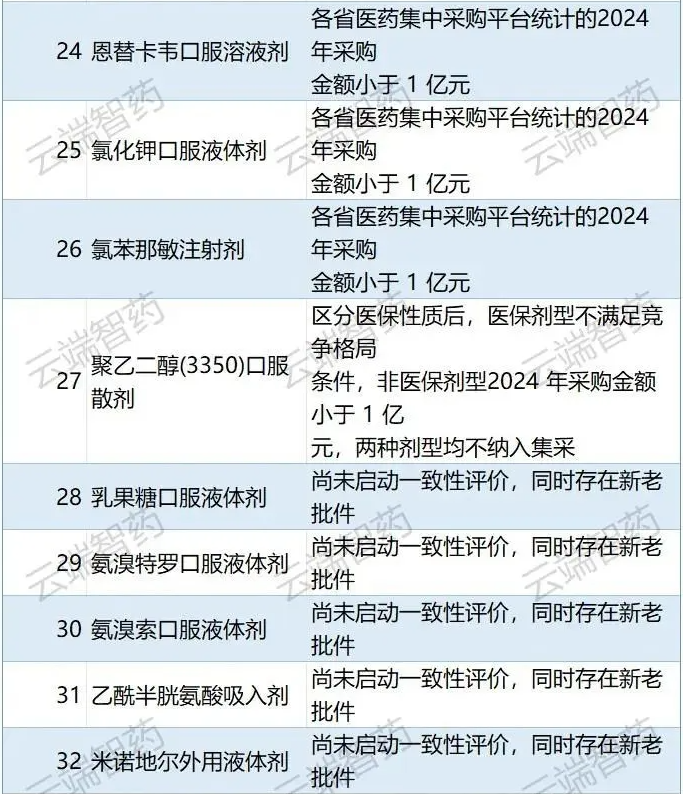
??? 三是2024年采購金額小于1億元的品種不納入,共排除他氟前列素滴眼劑、林可霉素注射劑等24個品種。國家組織藥品聯采辦與國家醫保局價采中心、首都醫科大學國家醫療保障研究院三方背對背測算各品種省級平臺采購金額,2024年采購金額小于1億元的品種不納入。
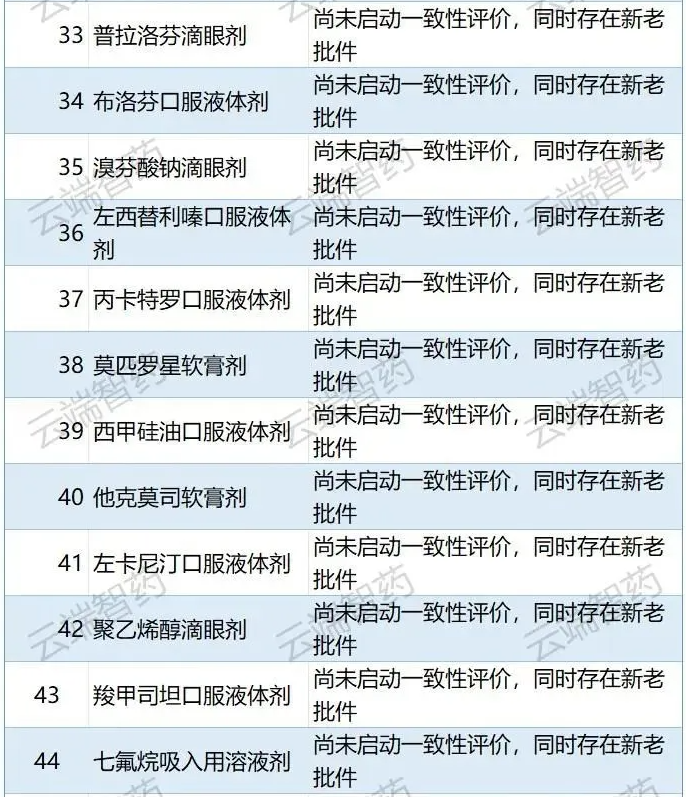
?? 四是尚未啟動一致性評價且新老批件并存的品種不納入,共排除他克莫司軟膏劑、利培酮口服液體劑等19個品種。
??? 目前藥監部門主要針對口服固體制劑和注射劑開展一致性評價工作,對口服溶液劑、吸入劑、滴眼劑、外用制劑等其他劑型的一致性評價工作方案正在研究中。
??? 這類劑型藥品中可能存在部分尚未開展一致性評價的老批件產品,以及部分近年來通過新注冊分類獲批的視同過評藥品,考慮到國家組織集采的投標產品須通過或視同通過一致性評價,為保障競爭的公平性,這類藥品不納入。
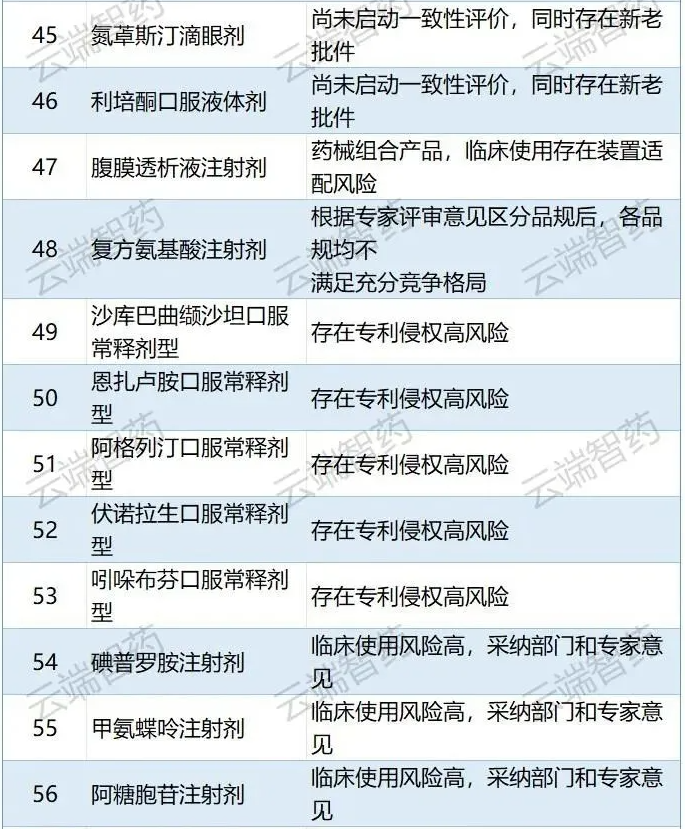
??? 五是存在裝置適配風險的藥械組合產品暫不納入,共排除腹膜透析液注射劑(含普通和低鈣)1個品種。
??? 該藥品屬于藥械組合產品,用于慢性腎功能衰竭透析。除藥品本身外,需配合醫療器械裝置使用,藥品包裝與裝置之間的適配性可能影響患者用藥安全。鑒于臨床使用等風險,不納入。排除上述情形的品種后,剩余75個品種。
??? 第二步:征求臨床醫學和藥學專家意見。
??? 鄭頤介紹,按照國家集采工作流程,國家組織藥品聯采辦于2025年5月13日在北京召開臨床和藥學專家咨詢會,從臨床使用和藥學特性等角度聽取專家意見,包括:品種是否適合納入本次集采、同品種不同品規間是否可替代、品種是否存在臨床使用其他風險等。
??? 結合臨床專家意見,主要成分相同但使用裝置、臨床使用場景、作用時效等不完全相同的,區分為不同品種集采,不滿足競爭格局的,不納入。
??? 共排除復方氨基酸注射劑1個品種以及丙卡特羅吸入劑等7個品種的部分品規,同時也有復方電解質注射劑1個品種區分后有2個品規均符合格局,按2個品種納入。
??? 如復方氨基酸注射劑包括15AA-Ⅱ、18AA-Ⅱ、18AA-Ⅶ、19AA-I、20AA等品規,臨床專家提出不同數字代表所含氨基酸種類數和配方不同,臨床使用場景有差異,需根據患者實際病情選擇,不能相互替代,參比制劑也不同,應作為不同品種進行集采。
??? 區分后,各品規競爭格局均不滿足條件,故未納入。綜合專家共識,剩余75個品種。
??? 第三步:根據相關部門及專家意見,進一步剔除存在相關風險的品種。
??? 一是專利尚未到期且知識產權承諾企業數不滿足遴選條件的品種暫不納入。
??? 結合相關部門意見和企業知識產權自主承諾情況,剔除阿格列汀口服常釋劑型、伏諾拉生口服常釋劑型、沙庫巴曲纈沙坦口服常釋劑型、恩扎盧胺口服常釋劑型、吲哚布芬口服常釋劑型等有重要專利尚未到期且知識產權承諾企業數不滿足遴選條件的5個品種。
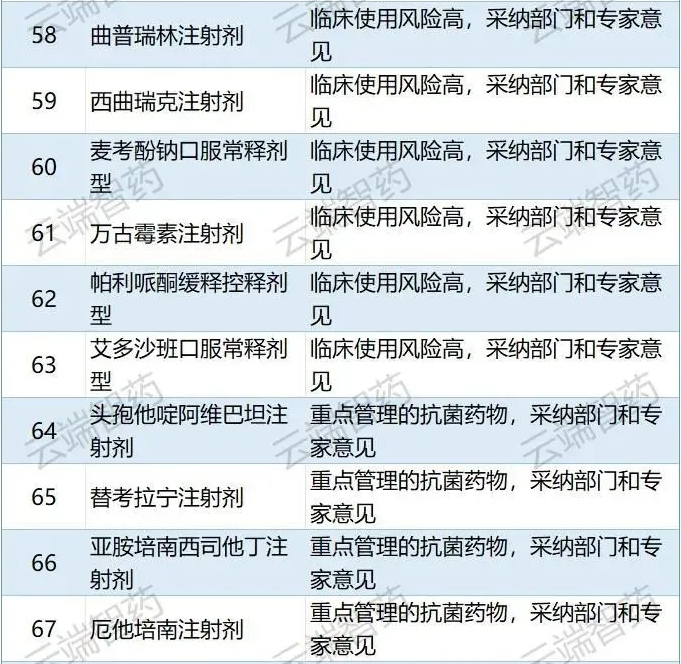
??? 二是臨床使用風險較高的品種不納入。
??? 采納相關部門和專家意見,剔除萬古霉素、麥考酚鈉、拉莫三嗪、碘普羅胺注射劑、甲氨蝶呤、曲普瑞林等14個臨床使用風險較高的品種。
??? 這些藥品是重點管理抗菌藥物、窄治療指數藥物、容易發生嚴重不良反應的藥物,以及輔助生殖技術相關藥物等,這類藥品對臨床診療經驗要求高、醫師和患者用藥習慣依從性強,為進一步保障集采結果平穩實施,暫不納入本次集采。
??? 例如,碘普羅胺注射劑(造影劑)屬于高警示藥物,易發生過敏性休克等嚴重不良反應,阿糖胞苷注射劑、甲氨蝶呤注射劑(白血病用藥)涉及鞘內注射,通過腰椎穿刺將藥物直接注入蛛網膜下腔,可能引發腦膜炎、顱內感染等,嚴重時危及生命。
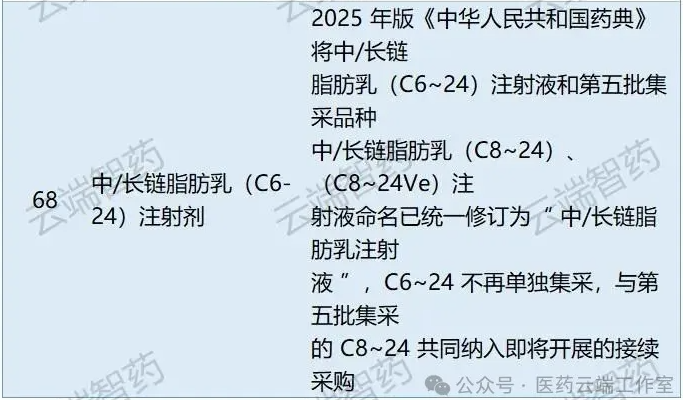
??? 另有中/長鏈脂肪乳(C6-24)1個品種,按照2025年版《中華人民共和國藥典》其命名將與中/長鏈脂肪乳注射液C8-24、C8-24Ve合并,統一稱為“中/長鏈脂肪乳注射液”。
??? 而C8-24Ve為第五批集采品種,將于近期進行接續采購。臨床醫生、藥師反映,上述品種在臨床上可相互替代,合并命名更有利于臨床用藥管理。
??? 因此,為平穩執行中選結果,中/長鏈脂肪乳(C6-24)注射液不再單獨納入第11批集采,與第五批集采品種中/長鏈脂肪乳(C8-24)、(C8-24Ve)注射液共同納入接續采購。
??? 鄭頤介紹,經過三個階段篩選,最終有55個品種納入第11批集采報量范圍。